非金属元素としての水素
水素は、非金属元素の中でも極めて重要な元素の1つです。周期表の一番左上、1族の第1周期に位置する元素です。
その性質について、図や式を用いながらわかりやすく解説します。また演習問題も用いて解説していきます。
本記事は以下のような人におすすめです!
- 水素の性質を確認したい。
それでは、始めましょう!
問題:水素
次の記述のうち、誤っているものを1つ選べ。
① 水素は、すべての気体のうちで最も軽く、水によく溶ける。
2021セミナー化学 | 第一学習社
② 水素は、還元作用を示し、加熱した酸化銅(Ⅱ)と反応して銅を生じる。
③ 水素は、酸素とともに燃料電池に用いられる。
④ 亜鉛に希硫酸を加えると、水素が発生する。
略解
①
テキスト:水素
まず、水素\(\mathrm{H}\)がどのような非金属元素であるか説明します。
水素は、宇宙で最も多く存在している元素で、水\(\mathrm{H_2O}\)や有機化合物の構成元素であり、自然界に多く分布していることが特徴としてあげられます。
水素の製法
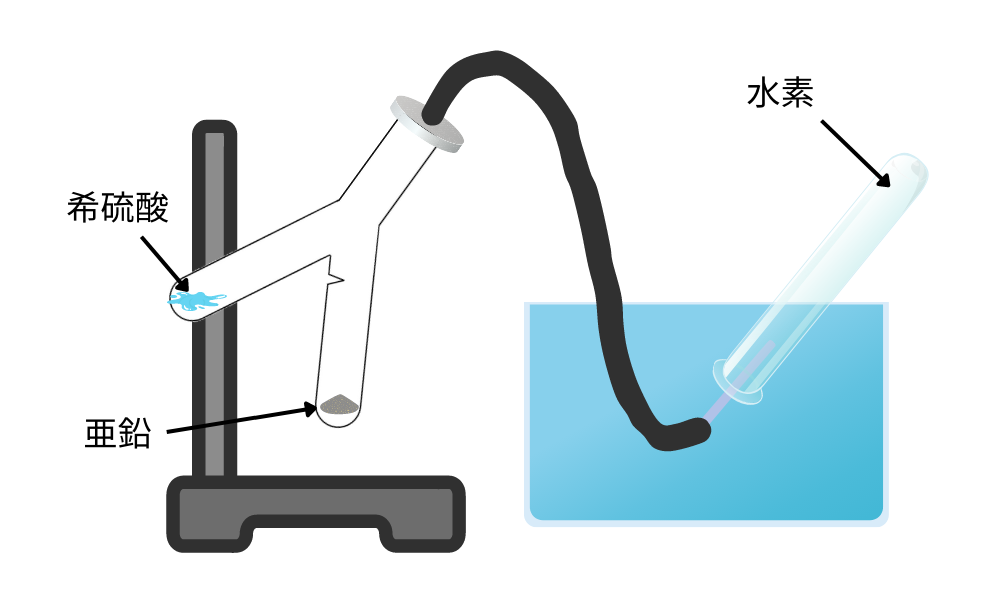
実験室では、亜鉛や鉄に希硫酸、希塩酸などの酸を加えて発生させて得ます。
水素は水に溶けにくいという性質があるので、右図のような水上置換法で採集します。
\(\mathrm{Zn + H_2SO_4 \rightarrow ZnSO_4 +H_2 \uparrow} \qquad (1) \)
また、水素はメタン\(\mathrm{CH_4}\)を高温の水蒸気と反応させることでも得ることができます。
\(\mathrm{CH_4 + H_2O \rightarrow CO + 3H_2 \uparrow} \qquad (2) \)
水素の性質
まず、水素の基本的な性質についてです。
| 融点 [℃] | -259 |
| 沸点 [℃] | -253 |
| 色/におい | 無色/無臭 |
| 密度※ [g/L] | 0.0899 |
水素の性質(データ)は表1のようになっています。
(※)0℃、1.013 Paでの値
- 状態:気体
- 常温では無色無臭
- すべての気体の中で最も密度が小さい
- 水に溶けにくい
- 空気中で点火すると炎を上げて燃える
また単体\(\mathrm{H_2}\)は二原子分子です。
水素の反応は主に2つあります。
- 1. 水素と酸素の混合気体に点火すると、爆発的に化合して水を生成する。
-
\(\mathrm{2H_2 + O_2 \rightarrow 2H_2O} \qquad (3) \)
- 2. 高温では還元剤として用いられる。
-
金属の酸化物を還元することができます。例えば、高温で酸化銅(Ⅱ)\(\mathrm{CuO}\)と反応して、銅\(\mathrm{Cu}\)を生じます。
\(\mathrm{CuO + H_2 \rightarrow Cu + H_2O} \qquad (4) \)
水素の用途
水素は主に2つの用途で使われます。
- 1. 水素化合物の合成原料となる。
-
塩化水素\(\mathrm{HCl}\)、アンモニア\(\mathrm{NH_3}\)、有機化合物などの合成原料となります。
- 2. 燃料電池の活物質として利用されている。
-
液体燃料式ロケットの燃料としても使われています。
水素化合物
水素と、他の元素との化合物を水素化合物といいます。水素は、貴ガス以外のほぼすべえての元素と水素化合物を作ります。
陽性の強い金属元素とは、水素化物イオン\(\mathrm{H^{-}}\)としてイオン結合をつくり、水素化ナトリウム\(\mathrm{NaH}\)、水素化カルシウム\(\mathrm{CaH_2}\)といった金属水素化物となります。
非金属元素との水素化合物は、共有結合からなる分子が多いです。
解説:水素
次の記述のうち、誤っているものを1つ選べ。
① 水素は、すべての気体のうちで最も軽く、水によく溶ける。
2021セミナー化学 | 第一学習社
② 水素は、還元作用を示し、加熱した酸化銅(Ⅱ)と反応して銅を生じる。
③ 水素は、酸素とともに燃料電池に用いられる。
④ 亜鉛に希硫酸を加えると、水素が発生する。
- ① 水素は、すべての気体のうちで最も軽く、水によく溶ける。
-
水素は水に溶けにくいです。(採集が水上置換で行えるのは水に溶けにくいからでした。)
- ② 水素は、還元作用を示し、加熱した酸化銅(Ⅱ)と反応して銅を生じる。
-
高温下で(4)式が成り立ちます。
- ③ 水素は、酸素とともに燃料電池に用いられる。
-
燃料電池の活物質として利用されています。
- ④ 亜鉛に希硫酸を加えると、水素が発生する。
-
水素の製法からわかります。(1)式が成り立つことからも説明できます。
A. ①
まとめ
水素の性質について解説しました。
本記事の重要事項を下記にまとめました。復習に役立ててください!
- 水素の製法について
- 水素の性質について
- 水素の用途について
- 水素化合物について
下記SNSにて、情報発信&質問対応を行っています。
質問については、本サイト内の内容に限らず勉強の相談等なんでもOKです。
本サイト運営者のかんたが直接お答えしております。お気軽にお問い合わせください!
X(旧Twitter)
LINE
Instagram
YouTube


質問・コメント