混合物の分離法が曖昧…?
 悩む人
悩む人昇華法の仕組みがイマイチよくわからない…
このような悩みで手が止まっていませんか?
昇華法に限らず、抽出、再結晶、クロマトグラフィー等でわからないところがある人は必見です。
今回は、
昇華法・抽出・再結晶・クロマトグラフィーを実践問題を通してわかりやすく解説していきます!
本記事は、以下のような人におすすめです!
- 昇華法の仕組みがわからない。
- 抽出の仕組みがわからない。
- 再結晶の仕組みがわからない。
- クロマトグラフィーの仕組みがわからない。



この記事を読んで、分離法を完璧にしよう!
ろ過・蒸留については下の記事をご覧ください!


問題1:昇華法
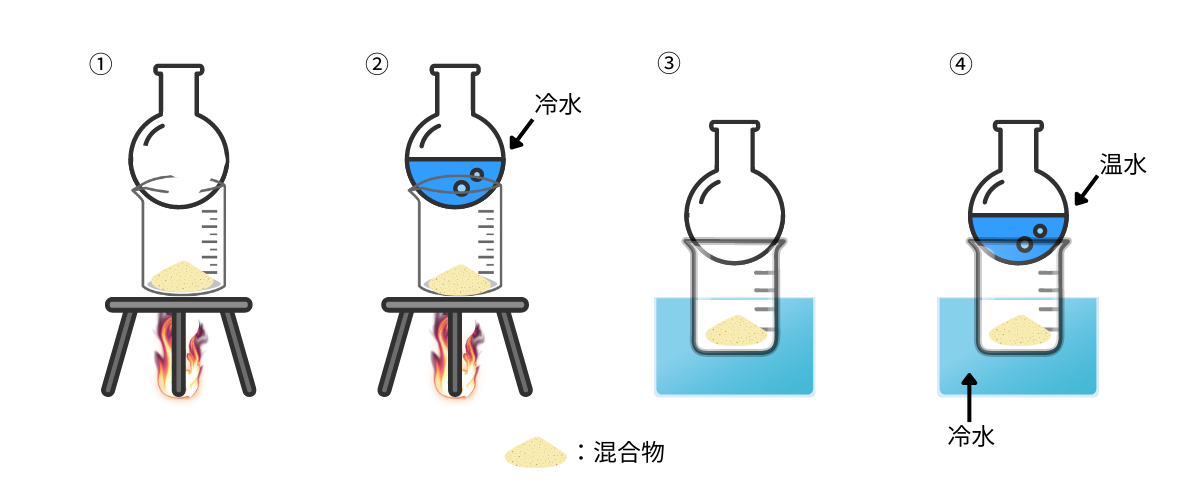
ガラスの破片が混じったヨウ素から、ヨウ素の昇華性を利用して、できるだけ多くのヨウ素を集めたい。最も適当な分離法を、次の①~④のうちから1つ選べ。
2020セミナー化学基礎 | 第一学習社
略解1
②
テキスト1:昇華法
昇華法というものが、どのようなものでどのように分離されるのかを説明します。
まず、昇華という言葉の意味を確認します。
あまり日常的に馴染みのあるものではないので、少し想像しにくいかも知れません。
具体例で考えてみましょう。
普通、氷などは加熱によって、氷→水→水蒸気というように液体を経由して個体から気体に変化します。
しかし、昇華性を示す物質は異なります。
ヨウ素(個体)は、加熱によってヨウ素(個体)→ヨウ素(気体)というように、変化中で液体を経由しません。
このような、個体から直接気体(またはその逆)に変化することを昇華というのです。
昇華という言葉がわかったところで、実際の昇華法を確認してみましょう。
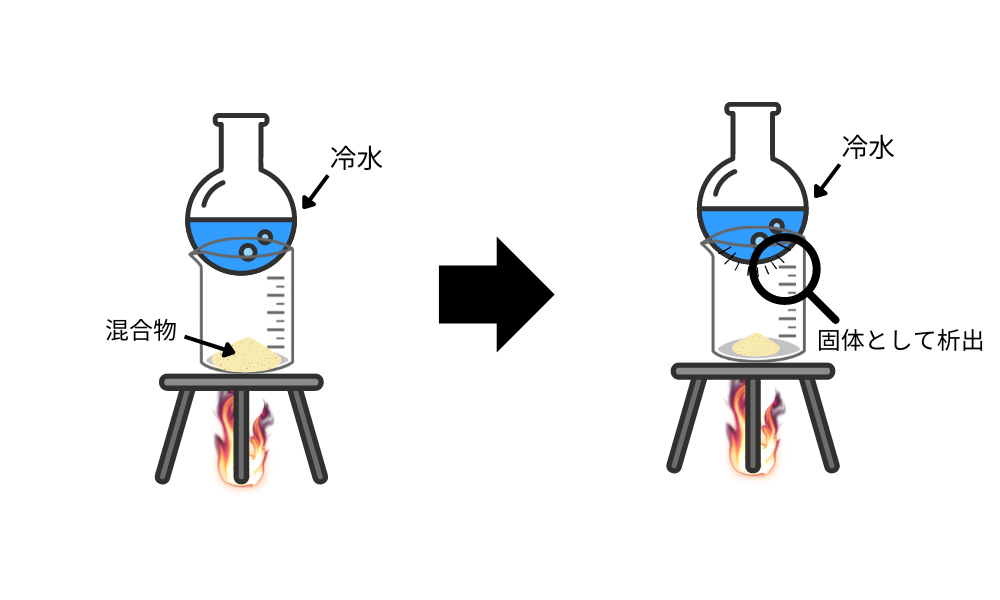

昇華法は、上記のような実験装置を用いて行われます。
昇華法の仕組みは以下のとおりです。
- 混合物を加熱すると、昇華性のある物質のみが昇華し気体となる。
- 昇華した物質が冷水の入ったフラスコの底面で再び固体として析出する。
一度気体になったものしか上部のフラスコには析出しないので、析出物は純粋な昇華性を示す物質であることがわかります。



昇華性を示す物質の代表例としてヨウ素、ナフタレンの2つが有名だよ。
これらを踏まえて、問題の解説を確認していきましょう。
解説1
ガラスの破片が混じったヨウ素から、ヨウ素の昇華性を利用して、できるだけ多くのヨウ素を集めたい。最も適当な分離法を、次の①~④のうちから1つ選べ。
2020セミナー化学基礎 | 第一学習社
①は冷却水がないため不適切です。
③と④はそもそも加熱されていないため、昇華性を示す物質を分離することはできません。



ヨウ素は昇華性を示すが、ガラスは昇華性を示さないため分離が可能だね。
A. ②
問題2:抽出
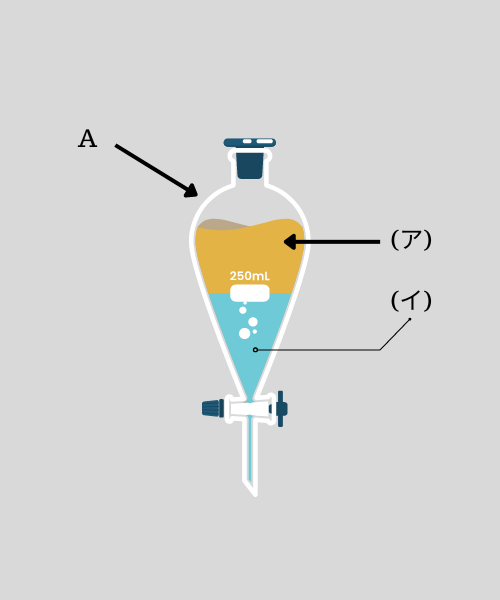
2020セミナー化学基礎 | 第一学習社ヨウ素とヨウ化カリウムとの混合溶液(ヨウ素液)がある。この混合溶液をガラス器具Aに入れ、さらにヘキサンを加えてよく振ったのち静置すると、図のように液体が2層に分かれた。このとき、上層(ア)は赤紫色になっていた。
(1)この分離法の名称を記せ。
(2)ガラス器具Aの名称を記せ。
(3)ヘキサン層は、図中の(ア)、(イ)のいずれか。
略解2
(1) 抽出
(2)分液ろうと
(3)(ア)
テキスト2:抽出
次は、抽出という分離操作について説明します。
まず、抽出の定義を見てみましょう。
抽出:溶媒を用いて、目的とする物質を固体や液体の中から分離する操作。
物質はそれぞれ溶媒への溶解のしやすさが異なります。
例えば、
コーヒーは溶媒である熱水に溶け出す香りや味を抽出しています。


では、抽出の実験操作について確認してみましょう。
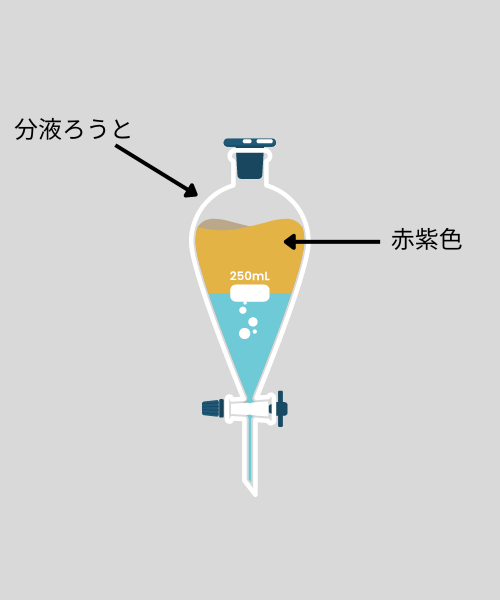

抽出操作では、上記のような分液ろうとという実験器具を用います。
分液ろうとは、溶媒への溶解のしやすさの違いを利用して物質を分離する手法です。
よって、溶媒に溶けやすいものが溶媒層に存在することになります。
溶媒に物質が溶けると、変色などの何らかの変化があるので、それに着目することが大切です。
これを踏まえて、抽出操作の解説を確認していきましょう。
解説2
2020セミナー化学基礎 | 第一学習社ヨウ素とヨウ化カリウムとの混合溶液(ヨウ素液)がある。この混合溶液をガラス器具Aに入れ、さらにヘキサンを加えてよく振ったのち静置すると、図のように液体が2層に分かれた。このとき、上層(ア)は赤紫色になっていた。
(1)この分離法の名称を記せ。
(2)ガラス器具Aの名称を記せ。
(3)ヘキサン層は、図中の(ア)、(イ)のいずれか。
- (1) この分離法の名称を記せ。
-
ヘキサン(溶媒)への溶けやすさによって混合水溶液を分離しているので、抽出です。
A. 抽出
- (2) ガラス器具Aの名称を記せ。
-
A. 分液ろうと(分液漏斗)
- (3) ヘキサン層は、図中の(ア)、(イ)のいずれか。
-
ヨウ素は、水に溶けにくくヘキサンに溶けやすい、という性質を持ちます。
ヨウ素を含むヨウ化カリウム水溶液(ヨウ素液)にヘキサンを加えて振り混ぜると、ヨウ素がヘキサン層に移動してヘキサン層が赤紫色になります。よって、(ア)の赤紫色の層がヘキサン層になります。A. (ア)
問題3:混合物の分離
次の(1)~(5)の分離操作に関連する分離法を、下の①~⑥から選び、番号で答えよ。
(1)少量の硫酸銅(Ⅱ)五水和物を含む硝酸カリウムから、硝酸カリウムの結晶だけを取り出す。
(2)液体空気の温度を徐々に上げていき、窒素だけを気体として取り出す。
(3)水性サインペンのインクをろ紙につけたのち、ろ紙の先端を水に浸し、インクに含まれる色素を分離する。
(4)塩化銀の沈殿を含む水溶液から、塩化銀を取り出す。
(5)茶葉に熱湯を加え、お茶に含まれる成分を湯に溶かし出す。
(分離法)
①ろ過、②再結晶、③クロマトグラフィー、④分留、⑤昇華法、⑥抽出
セミナー化学基礎2020 | 第一学習社
略解3
(1)②
(2)⑤
(3)③
(4)①
(5)⑥
テキスト3:混合物の分離
最後に、分離法全6種類のうち残った再結晶、クロマトグラフィーについて説明します。
まず、再結晶から見ていきましょう。
まず、結晶という言葉について確認します。
大雑把に言うと、結晶とは固体のことを指します。
そして、再結晶とは名前の通り、再び結晶にする→再び固体にする、ということです。
ここで、再結晶の定義を見てみましょう。
再結晶:不純物が混じった固体を熱水などに溶かし、冷却すると、ほぼ純粋な結晶をとり出す事ができる。この操作を再結晶という。
再結晶は、物質における溶解度(一定量の溶媒に溶解する量)の違いを利用します。
例えば、
熱水に解けた不純物を含む硝酸カリウム水溶液を冷やすと、硝酸カリウムの溶解度は小さいので不純物より先に析出します。
その析出物を取り出すと、純粋な硝酸カリウムだけが得られるということです。
次に、クロマトグラフィーも確認します。
クロマトグラフィーは主に有機化学で登場することが多い分離法です。
クロマトグラフィー:溶媒に溶かした物質がろ紙やシリカゲルなどの吸着剤の上を移動(展開)する際に、物質による吸着力の違いで、移動速度が異なる。これを利用した分離法を、クロマトグラフィーという。
また、クロマトグラフィーは用いる吸着剤によって以下のように名前がつけられています。
| 名称 | 吸着剤 |
| ペーパークロマトグラフィー | ろ紙 |
| カラムクロマトグラフィー | シリカゲルなどをカラムに詰めて用いる |
| 薄層クロマトグラフィー | 吸着剤を硝子板等の上に薄くのばしたもの |



うーん、全くイメージが湧かないなぁ…
定義だけ述べられても想像しにくいと思います。
そこで、ペーパークロマトグラフィーを例にその原理をわかりやすく説明します。
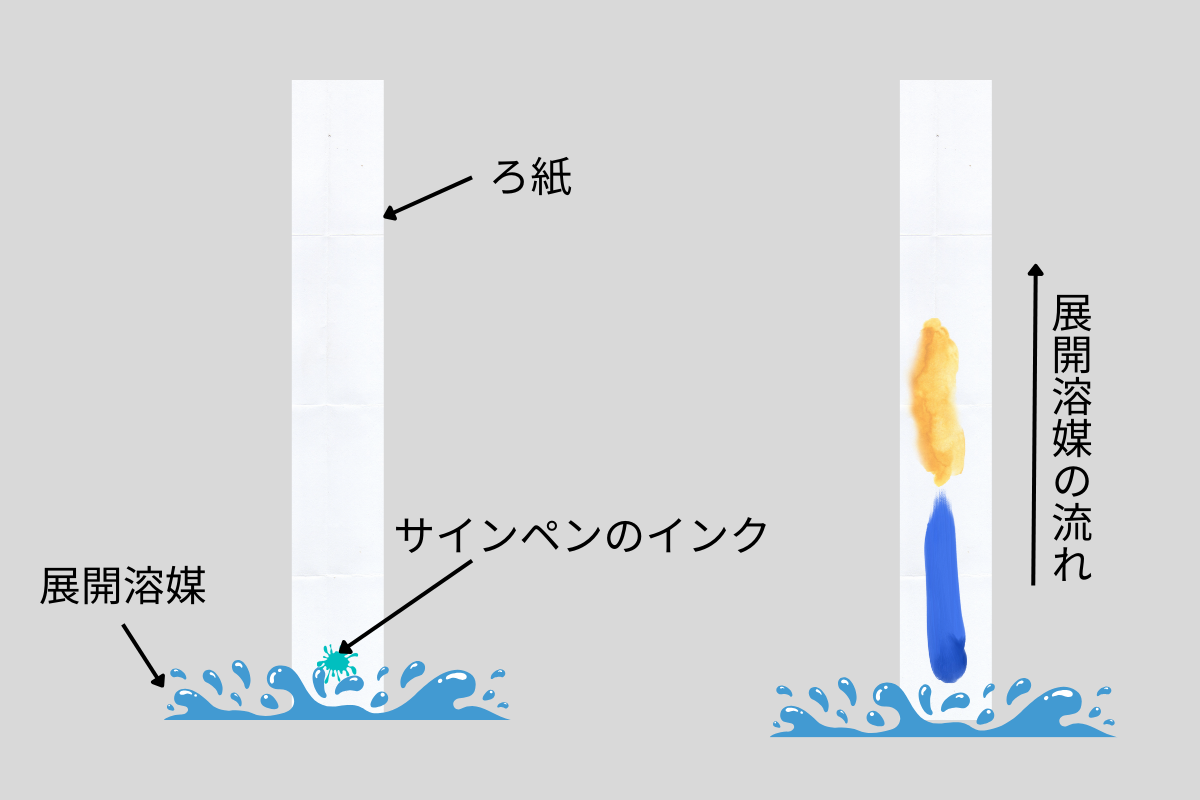

ペーパークロマトグラフィーは、吸着剤にろ紙を用いて行います。
手順は次のとおりです。
- ろ紙にサインペンのインクを垂らして、それを展開溶媒に浸ける。
- ろ紙が展開溶媒(液体)を吸い上げます。
- ろ紙との吸着力が弱い黄色インクは水と一緒に流れて上がっていく。
- ろ紙との吸着力が強い青色インクは水によってあまり流れずその場にとどまる。
展開溶媒にろ紙を浸けると、徐々に水が染み込んで上がっていくのが想像できると思います。
それと一緒にインクも上がるのですが、ろ紙との摩擦が大きい青色インクはあまり上がりません。
一方、ろ紙との摩擦が小さい黄色インクは水と一緒にぐんぐん上がります。
そうすると、最終的に青色インクと黄色インクを分離することができました。



図を見ると、クロマトグラフィーの原理がイメージできるね!
最後に、蒸留の仲間の分留について説明したいと思います。
分留(分別蒸留):液体の混合物を沸点の佐を利用して蒸留によって成分ごとに分ける操作。
蒸留では、蒸発した気体をリービッヒ冷却器で冷却して液体として回収していました。
しかし、分留は蒸発した気体をそのまま気体として回収する方法です。
例えば、
原油をガソリン、灯油、軽油に分類する操作、
液体空気を窒素と酸素に分ける操作、
などがあります。
ろ過・蒸留についてはこの記事で解説していません。
もし、この2つの分離法についておさらいしたい場合は下記記事をチェックしてみてください。


これらを踏まえて、問題解説を確認していきましょう。
解説3
次の(1)~(5)の分離操作に関連する分離法を、下の①~⑥から選び、番号で答えよ。
(1)少量の硫酸銅(Ⅱ)五水和物を含む硝酸カリウムから、硝酸カリウムの結晶だけを取り出す。
(2)液体空気の温度を徐々に上げていき、窒素だけを気体として取り出す。
(3)水性サインペンのインクをろ紙につけたのち、ろ紙の先端を水に浸し、インクに含まれる色素を分離する。
(4)塩化銀の沈殿を含む水溶液から、塩化銀を取り出す。
(5)茶葉に熱湯を加え、お茶に含まれる成分を湯に溶かし出す。
(分離法)
①ろ過、②再結晶、③クロマトグラフィー、④分留、⑤昇華法、⑥抽出
セミナー化学基礎2020 | 第一学習社
- (1)少量の硫酸銅(Ⅱ)五水和物を含む硝酸カリウムから、硝酸カリウムの結晶だけを取り出す。
-
硝酸カリウムは溶解度が小さいのが特徴で、再結晶で取り出すことができます。
A. ②
- (2)液体空気の温度を徐々に上げていき、窒素だけを気体として取り出す。
-
温度を上げたときに蒸発しやすい窒素だけを取り出しているので分留です。
A. ④



液体(空気)→気体(窒素)を取り出すから⑤昇華法じゃないの?



窒素は昇華性を示さないから、昇華法では分離できないよ!
- (3)水性サインペンのインクをろ紙につけたのち、ろ紙の先端を水に浸し、インクに含まれる色素を分離する。
-
テキスト3で示した具体例の通り、これはろ紙への吸着力の違いを利用したペーパークロマトグラフィーです。
A. ③
- (4)塩化銀の沈殿を含む水溶液から、塩化銀を取り出す。
-
固体と液体を分離する操作はろ過です。
A. ①
- (5)茶葉に熱湯を加え、お茶に含まれる成分を湯に溶かし出す。
-
特定の成分を溶媒に溶かして分離するため抽出です。
A. ⑥
まとめ
昇華法、抽出、再結晶、クロマトグラフィーの4種類の分類について解説しました。
ろ過・蒸留の2つの分離法と合わせて合計6つの分離法は非常に重要なので是非マスターしてください。
本記事の重要事項を以下にまとめました。復習に役立ててください!
抽出:溶媒を用いて、目的とする物質を固体や液体の中から分離する操作。
再結晶:不純物が混じった固体を熱水などに溶かし、冷却すると、ほぼ純粋な結晶をとり出す事ができる。この操作を再結晶という。
クロマトグラフィー:溶媒に溶かした物質がろ紙やシリカゲルなどの吸着剤の上を移動(展開)する際に、物質による吸着力の違いで、移動速度が異なる。これを利用した分離法を、クロマトグラフィーという。
下記SNSにて、情報発信&質問対応を行っています。
質問については、本サイト内の内容に限らず勉強の相談等なんでもOKです。
本サイト運営者のかんたが直接お答えしております。お気軽にお問い合わせください!
X(旧Twitter)
LINE
Instagram
YouTube


質問・コメント